Redakcja Bieganie.pl
Wzrastające zakwaszenie w czasie wysiłków fizycznych tradycyjnie zwykło się tłumaczyć zwiększoną produkcją kwasu mlekowego, który uwalniając proton H+ doprowadza do spadku PH. Jeżeli ilość wolnego protonu H+ przekroczy wewnątrzkomórkowe systemy buforujące dochodzi do wzrostu zakwaszenia i objawowej kwasicy metabolicznej. Według tej teorii jedną z wielu przyczyn ograniczających możliwości wysiłkowe mięśnia w czasie intensywnej pracy jest właśnie wzrost stężenia mleczanu, prowadzący do wewnątrzkomórkowej kwasicy. Tradycyjna interpretacja bazuje na fakcie, iż kwas mlekowy jest stosunkowo silnym kwasem organicznym (pKa=3,87), który w środowisku komórkowym występuje w całkowicie zdysocjowanej formie. Uwolnione protony H+ doprowadzają właśnie do wystąpienia kwasicy metabolicznej zwanej również, od rzekomego dawcy protonów, kwasicą mleczanową.
Jako pierwszy istnienie kwasu mlekowego odkrył w 1780 roku szwedzki chemik Carl Wilhelm Scheele. Jego obecność stwierdził w próbkach kwaśnego mleka, co było powodem do nadania "nowej" cząsteczce nazwy kwas mlekowy (właściwa nazwa chemiczna to kwas 2-hydroksypropanowy). Dwaj laureaci nagrody Nobla w 1922 roku Otto Meyerhoff i Archibald V. Hill byli pionierami badań nad biochemią wysiłków fizycznych. Ich badania nad utlenianiem węglowodanów pokazały, iż w warunkach niedoboru tlenu utlenianie glukozy prowadzi do powstania kwasu mlekowego. Kwas mlekowy powstaje również w czasie kiedy nagle wzrasta zapotrzebowanie energetyczne pracującego mięśnia, a źródła dostarczania substratów energetycznych przy udziale procesów tlenowych nie są wystarczające. Stwierdzenie obecności kwasu mlekowego w pracującym mięśniu dało podstawę do wysnucia teorii o przyczynie rozwoju kwasicy metabolicznej, której to bezpośrednią przyczyną ma być narastające stężenie kwasu mlekowego. Na bazie tego poglądu przeprowadzano wiele eksperymentów, które miały potwierdzić założoną tezę. Wyniki jednego z nich zaprezentowano poniżej.
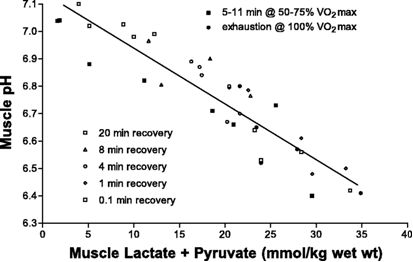
Wykres przedstawia liniową zależność między sumą zmierzonych stężeń mleczanu i pirogronianu wobec spadku PH (wzrostu zakwaszenia) w czasie wysiłków o różnej intensywności oraz przy różnym czasie wypoczynku. Taka zależność jest tylko dowodem na istnienie związku przyczynowo skutkowego między ilością mleczanu powstającego w czasie glikolizy, a współistniejącym zakwaszeniem mięśni, nie wskazuje jednak bezpośrednio na źródło pochodzenia protonów będących przyczyną rozwoju kwasicy metabolicznej.
Kwasica metaboliczna nie jest wynikiem samego uwolnienia protonu H+, jej wystąpienie warunkuje zaburzenie równowagi pomiędzy uwolnieniem protonu H+ a jego utylizacją i możliwością buforowania. Nie ma biochemicznych podstaw aby stwierdzić, iż kwas mlekowy (właściwie mleczan) jest przyczyną kwasicy metabolicznej. Więcej, istnieją badania, które pokazują, że powstawanie mleczanu pomaga wręcz zapobiegać kwasicy. Przeprowadzono eksperyment na izolowanym mięśniu sercowym fretki. Badano zakwaszenie po zablokowaniu fosforylacji oksydatywnej oraz glikolizy. Wykazano znacznie szybciej postępującą kwasicę w czasie kiedy glikoliza była całkowicie zablokowana, niż kiedy tylko zablokowano przemiany mitochondrialne. To daje podstawy aby stwierdzić, iż to nie produkt glikolizy jakim jest mleczan doprowadza do zakwaszenia. Jest ono wynikiem nasilonej hydrolizy ATP i brakiem możliwości utylizacji uwolnionego protonu w mitochondrialnym łańcuchu oddechowym. Mleczan, jego powstawanie, nie jest przyczyną tylko skutkiem, który wręcz pomaga opóźnić jak również zmniejszyć wystąpienie negatywnych skutków gwałtownych przemian energetycznych w pracującym mięśniu. Ponadto, badając ilość uwolnionego protonu H+ w stosunku do ilości zmierzonego mleczanu zaobserwowano, iż nieproporcjonalnie więcej protonów zostaje uwolnionych niż wynikałoby to ze stosunku dysocjacji kwasu mlekowego. Sytuacja ta zaprezentowana jest na poniższym wykresie.
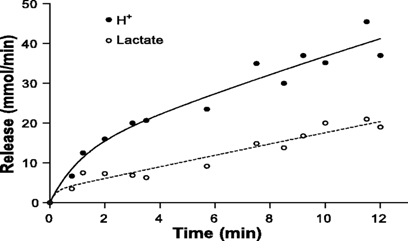
Kolejny wykres, tym razem słupkowy, przedstawia zestawienie wielkości uwolnionego protonu na podstawie zmierzonej ilości powstałego mleczanu, przy założeniu, że dochodzi do rzekomej dysocjacji kwasu mlekowego, wobec pojemności systemów buforujących w komórce. Jak widać, ilość uwolnionego mleczanu (protonu H+) jest zdecydowanie za mała aby wywołać zakwaszenie, gdyż jest znacznie poniżej możliwości buforów komórkowych. W takiej sytuacji nie dochodzi do zakwaszenia pomimo uwolnienia mleczanu.
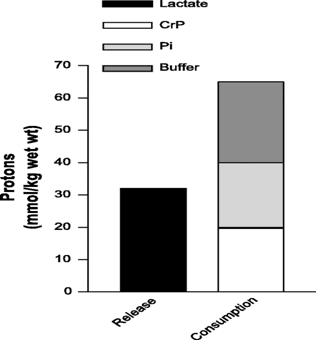
Idąc dalej tym porównaniem, zestawiono ilości uwolnionego protonu w czasie hydrolizy ATP oraz w czasie glikolizy do pojemności buforów komórkowych, pośród których uwzględniono bufory statyczne oraz tak zwane czynnościowe – mleczan i fosfokreatynę. Takie zestawienie daje niemal identyczne słupki z niewielką przewagą strony lewej, która oznacza uwolnienie protonu. Tym samym otrzymujemy obraz sytuacji gdzie zostaje zaburzona równowaga między uwolnieniem protonu, a jego zbilansowaniem w następstwie czego dochodzi do rozwoju zakwaszenia wewnątrzkomórkowego.
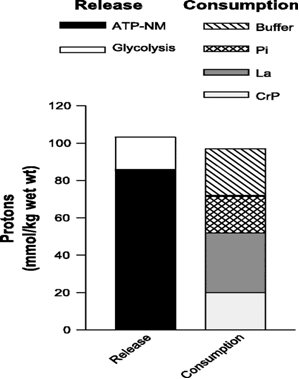
Trzeba sobie również uświadomić, jakie są możliwości regeneracji zasobów energetycznych (ATP) komórki mięśniowej. Pomimo „dużej ekonomiki” przemian mitochondrialnych, ich możliwości dostarczania energii są znacznie ograniczone w stosunku do możliwości przemian glikolitycznych czy też reakcji kinazy kreatynowej. Dlatego możliwa jest sytuacja, kiedy nasilona praca doprowadza do wyczerpania możliwości dostarczania energii przez system mitochondrialny, a deficyt energetyczny pokrywany zostaje przez cytozolowe przemiany: glikolizę oraz reakcję kinazy kreatynowej.
|
System Energetyczny |
Maksymalna ilość syntezy ATP |
|
Cytozol |
|
|
Fosfokreatyna |
2.4 |
|
Glikoliza |
1.3 |
|
Mitochondria |
|
|
Utlenianie glukozy |
0.7 |
|
Utlenianie kwasów |
0.3 |
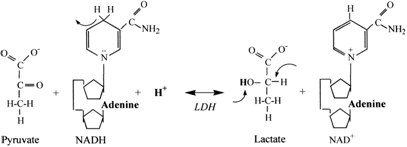
Kwasica metaboliczna powstaje w wyniku nasilonej utylizacji zasobów ATP połączonej ze wzrostem udziału glikolizy w resyntezie ATP. Na potrzeby pracy komórki mięśniowej zostaje uwolniona energia w czasie hydrolizy bogatoenergetycznego wiązania fosforanowego cząsteczki ATP. Powstałe ADP oraz reszta fosforanowa Pi są bezpośrednio włączane w cykl przemian glikolitycznych gdzie następuje resynteza ATP. W czasie glikolizy zredukowaniu ulega NAD+ do formy NADH oraz powstają protony. W warunkach wydolności mitochondrialnego systemu pozyskiwania energii powstały NADH oraz protony H+ są przekazywane na łańcuch oddechowy gdzie są utylizowane przy udziale tlenu. W czasie niedoboru tlenu lub znacznego zapotrzebowania na energię (bardzo nasilonej pracy mięśniowej), przekraczającego możliwości systemu mitochondrialnego, pula zredukowanego nukleotydu NADH jest reoksydowana w czasie reakcji przekształcenia pirogronianu w mleczan. W tej reakcji również są przyłączane dwa protony H+ co zapobiega lub opóźnia wystąpienie kwasicy.
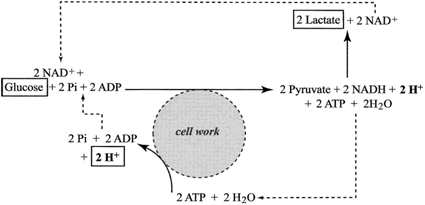
Jak widać z przedstawionego schematu to niezbilansowane protony H+ powstające w wyniku hydrolizy ATP mają bezpośredni wpływ na kwasowość środowiska komórkowego. Można więc powiedzieć, iż kwasica metaboliczna rozwija się na skutek nasilenia przemian energetycznych komórki, a jej bezpośrednią przyczyną jest przebieg cytozolowych (pozamitochondrialnych) reakcji hydrolizy ATP.
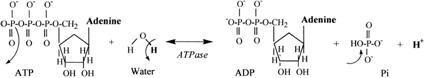
W czasie hydrolizy ATP zostaje uwolniony proton H+ oraz reszta fosforanowa, która wykazuje duży potencjał do buforowania (przyłączania) protonów H+. Nie można jednak wyrównać (zbuforować) nadmiaru protonów H+ powstałych w reakcji hydrolizy ATP przez powstające jednoczenie reszty fosforanowe, gdyż te na bieżąco są zużywane do resyntezy ATP w czasie glikolizy oraz przez mitochondrialny łańcuch oddechowy. Ilość wolnych fosforanów jest więc nieproporcjonalnie mniejsza od ilości protonów H+ powstałych w wyniku hydrolizy ATP dlatego ich zdolność do buforowania jest znacznie mniejsza niż wynika to z przebiegu reakcji hydrolizy ATP.
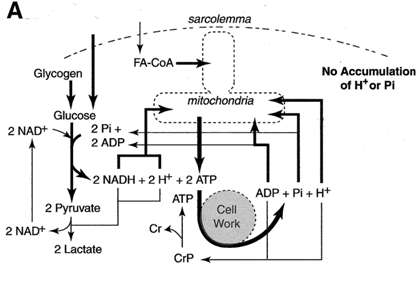
Mówiąc o pozamitochondrialnych przyczynach kwasicy trzeba wiedzieć, że to właśnie ograniczenia przemian w obrębie mitochondriów doprowadzają do zaburzenia utylizacji protonów H+ i do następującego rozwoju kwasicy w wyniku ich nagromadzenia. W tak zwanym „stanie spoczynkowym”, kiedy zapotrzebowanie energetyczne komórki mięśniowej pozostaje na względnie niskim poziomie, nie dochodzi do kumulacji protonów gdyż te przekazywane są właśnie do mitochondriów gdzie są wykorzystywane do wytworzenia energii (ATP) w obrębie łańcucha oddechowego. Również pula zredukowanego nukleotydu NADH jest regenerowana w mitochondrium. Zostaje zachowana równowaga w bilansie dostarczania i utylizacji protonów H+.
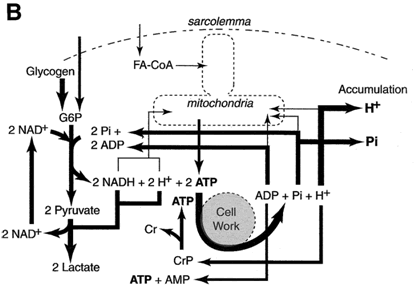
Reakcja dehydrogenazy mleczanowej pozwala na odbudowanie zasobów NAD+ niezbędnych dla kontynuowania glikolizy w warunkach kiedy system mitochondrialny jest już niezdolny do przyjmowania „ponad miarę” substratów dla swoich przemian energetycznych.
Kwasica metaboliczna jest zjawiskiem groźnym dla homeostazy organizmu bez względu na przyczynę jej powstawania. Z praktycznego punktu widzenia nie ma różnicy czy jest ona następstwem działania ATP-azy hydrolizującej ATP na potrzeby pracy mięśniowej, czy wynikiem nasilonej glikolizy. Kwasica jest niewątpliwie jednym z czynników ograniczających maksymalne wysiłki fizyczne. Ważne jednak aby prowadząc różnego rodzaju dywagacje na temat progu mleczanowego mieć świadomość, iż powstający mleczan sam w sobie nie jest zły. Nie jest tak, że organizmowi jest ciężko go „tolerować”, a to z kolei przyczynia się do rozwoju zmęczenia mięśniowego. Mleczan, jego droga powstawania, jest swego rodzaju wyjściem awaryjnym ratującym mechanizmy energetyczne przed całkowitym załamaniem. Warunkuje to możliwość przedłużenia okresu tak zwanej pracy na długu energetycznym oraz daje pełną niezależność od metabolizmu mitochondrialnego (tlenowego). W porównaniu do przemian cyklu Krebsa glikoliza jest znacznie bardziej wydajnym systemem dostarczania energii, zwłaszcza kiedy ta jest niezbędna szybko i w znacznych ilościach. Bilans mleczanu we krwi jest dobrym pośrednim wskaźnikiem zakwaszenia ustroju i daje swego rodzaju obraz o źródłach energetycznych zużywanych do pozyskania energii przy zadanej intensywności pracy. Kumulacja mleczanu świadczy bowiem o przekroczeniu możliwości dostarczania ATP przy pomocy metabolizmu mitochondrialnego, który jak wiadomo jest niezwykle ekonomiczny, a dla długodystansowca jest szczególnie ważną sprawą oszczędna gospodarka substratami węglowodanowymi ze względu na ich ograniczone możliwości magazynowania.
ŹRÓDŁO: Biochemistry of exercise-induced metabolic acidosis, Robert A. Robergs,1 Farzenah Ghiasvand and Daryl Parker Science Program, California State University-Sacramento, Sacramento, California:
http://ajpregu.physiology.org/cgi/reprint/287/3/R502